Comentari per part de la Dra. Marta Vives Pi sobre l’article "Teplizumab and β-Cell Function in Newly Diagnosed Type 1 Diabetes" de Eleanor L Ramos et al, oct 18, 2023. The New England Journal of Medicine (NEJM). DOI: 10.1056/NEJMoa2308743
Al novembre de 2022, la FDA va aprovar Teplizumab, el primer fàrmac que retardava el diagnòstic de la diabetis tipus 1 (DT1), una malaltia autoimmunitària causada per la destrucció de les cèl·lules beta pancreàtiques productores d’insulina. Teplizumab és un anticòs monoclonal anti-CD3 y es va demostrar que frenava la destrucció de les cèl·lules beta en individus amb alt risc de desenvolupar DT1, retardant 2 anys l’aparició de símptomes clínics. Els resultats es van publicar al New England Journal of Medicine el 15 d’agost de 2019 per part del Type 1 Diabetes TrialNet Study Group (https://www.nejm.org/doi/full/10.1056/nejmoa1902226). Aquesta teràpia pionera demostrava la capacitat del fàrmac per frenar l’autoimmunitat preservant temporalment les cèl·lules beta remanents. Tot i no prevenir la malaltia, el retard en l’aparició dels símptomes clínics incideix en la qualitat de vida i en les futures complicacions secundàries dels pacients.
Posteriorment es va posar en marxa un assaig clínic (Fase 3) per avaluar l’eficàcia i seguretat de Teplizumab en nens i adolescents amb DT1 acabada de diagnosticar (https://clinicaltrials.gov/ct2/show/study/NCT03875729).El passat 19 d’octubre, la revista New England Journal of Medicine en publicava els resultats (https://www.nejm.org/doi/pdf/10.1056/NEJMoa2308743).
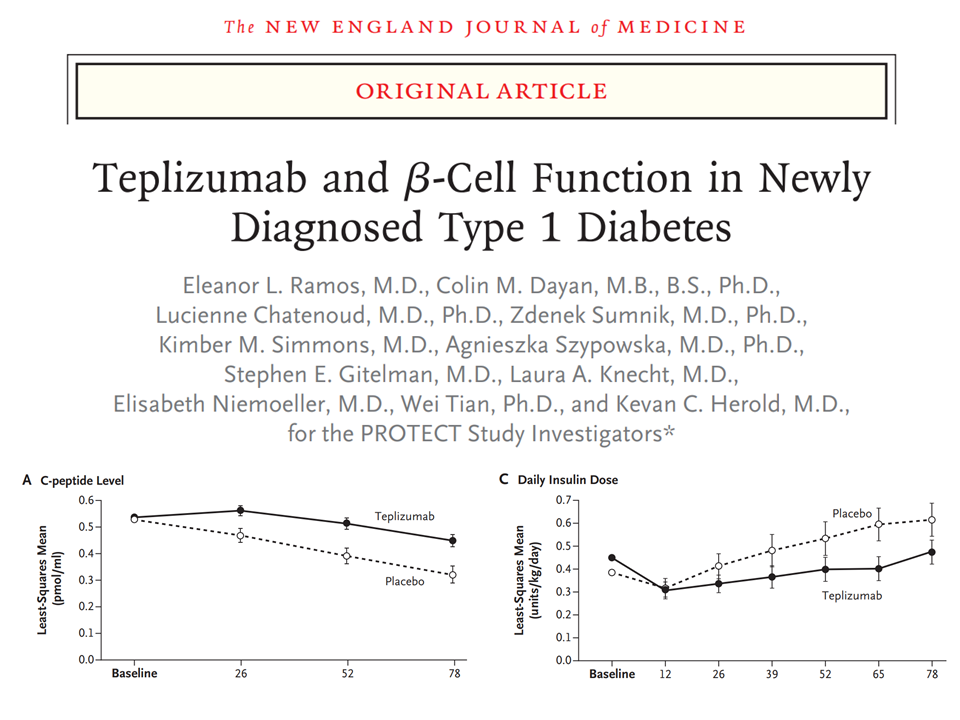
En l’assaig, dut a terme durant la pandèmia de Covid-19, han participat 328 nens i adolescents (entre 8 i 17 anys) amb DT1 diagnosticada en les 6 setmanes anteriors. Després del tractament, els pacients que havien rebut Teplizumab (n=217) tenien nivells significativament superiors de C-pèptid que els del grup placebo (n=111). El C-pèptid és una molècula que s’escindeix de la proinsulina quan se secreta la insulina; per tant, és una mesura precisa de la insulina que produeix el pàncrees. Malgrat això, els dos grups no eren diferents en quant a paràmetres metabòlics com la dosi d’insulina diària injectada, la concentració de glucosa en sang i l’hemoglobina glicada. Els efectes adversos eren deguts a l’administració del fàrmac (6.9% dels pacients) o del placebo (2.7 dels pacients) destacant alteracions en la producció de citocines, cefalea, molèsties gastrointestinals, limfopènia, infeccions i erupcions cutànies.
Els resultats demostren un cert benefici de Teplizumab en preservar la funció de les cèl·lules beta remanents de manera perllongada. Els autors especulen que el mecanisme d’acció pot ser induint cèl·lules T CD8+ exhaustes, entre les que estarien les auto-reactives. El fàrmac s’administra de manera intravenosa durant 12 dies i en dos cicles, i la recuperació dels efectes secundaris és ràpida sense observar-se immunosupresió al final del tractament. Com a limitacions de l’assaig cal destacar el fet de no ser una teràpia antigen-específica i els efectes adversos sobre el sistema immunitari. No s’ha determinat la immunogenicitat del fàrmac, com ara l’aparició d’anticossos anti-teplizumab en els pacients tractats. Seria interessant conèixer l’efecte de Teplizumab en adults amb DT1, ja que solen tenir formes menys agressives de la malaltia i també en un grup amb representació ètnica més àmplia.
Tot i les limitacions de l’assaig i la manca d’efecte en els paràmetres metabòlics de la diabetis, els resultats demostren que es pot recuperar parcialment la producció d’insulina endògena amb 2 cicles Teplizumab.
Dra. Marta Vives Pi [Immunology Department, Germans Trias i Pujol Research Institute (IGTP), Autonomous University of Barcelona (UAB)].