Comentari per part de la Dra. Jennifer Bolaños sobre la notícia publicada a La Vanguardia:
El sistema Complement al rescat de la forma més freqüent de degeneració macular associada a l'edat (DMAE)
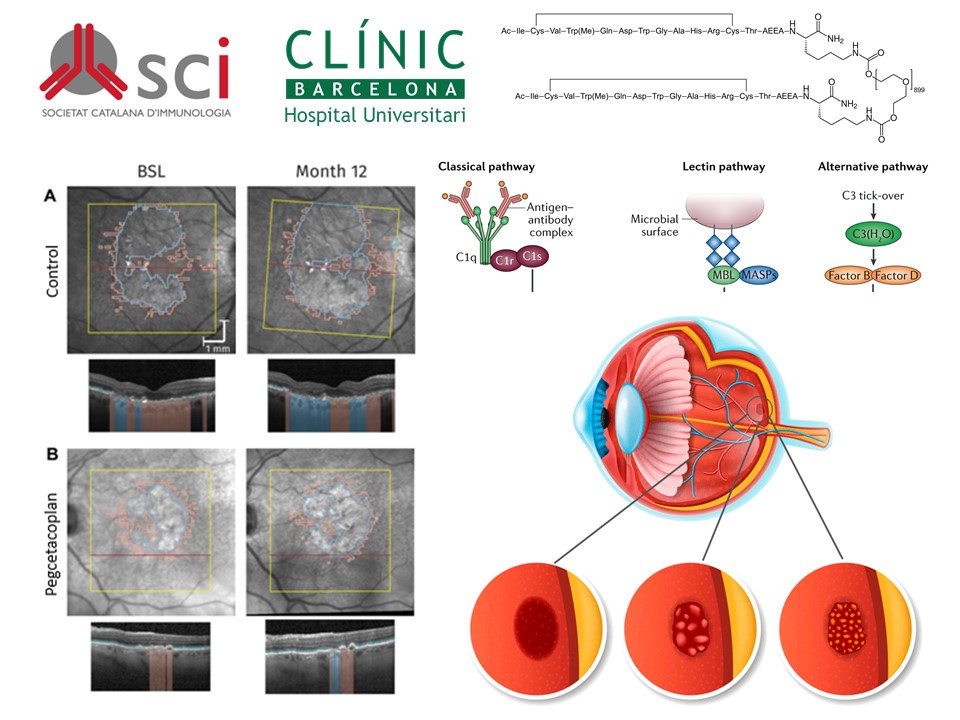
La DMAE és una pèrdua gradual de la visió central responsable de la principal causa de ceguesa en més grans de 50 anys especialment en països desenvolupats. Es calcula que a Espanya unes 700.000 persones (1,5 de la població actual) pateixen aquesta malaltia i s'espera que aquest nombre augmenti en el futur. Tot i que el mecanisme responsable de l'inici i la progressió d'aquesta malaltia és poc conegut, hi ha anàlisis histopatològiques i estudis experimentals in vitro i in vivo que han associat la patogènesi a la presència d'inflamació crònica i hiperactivació del sistema del complement. Aquest darrer és un component principal de la immunitat innata, constituït per un conjunt de proteïnes sèriques que s'activen en cascada per generar respostes inflamatòries encaminades a eliminar elements nocius per al nostre organisme (microorganismes, proteïnes o cèl·lules alterades, etc.)
La DMAE en estadis primerencs i intermedis es caracteritza per la presència de druses que són dipòsits extracel·lulars d'una sèrie de proteïnes i que estan localitzats entre l'epiteli pigmentari de la retina (EPR) i la membrana de Bruch. Aquests dipòsits estan compostos principalment per lipoporoteïnes i fragments d'alguns components centrals del sistema Complement com són C3 i C5, cosa que suggereix l'existència d'inflamació crònica local al nivell del complex EPR-membrana de Bruch que podrien estar jugant un paper important en el desenvolupament de les druses i per tant de la DMAE.
Hi ha dos tipus de DMAE avançada: l'exudativa o “humida” que és la forma més greu i, afortunadament, menys freqüent (~10%) i la no exudativa o “seca” més lleu, encara que també incapacitant, i més freqüent (~ 90%). Mentre que per a la primera ja hi ha fàrmacs aprovats, la segona no comptava fins ara amb l'aprovació de cap malgrat la realització de múltiples assaigs clínics que incloïen fàrmacs amb diferents mecanismes d'acció com Brimonidine, Fenretinide, Emixustad, anticossos monoclonals contra beta amiloide entre d'altres. En base a estudis que donen suport a la possibilitat d'hiperactivitat del sistema Complement com a promotora de lesions força freqüents en la forma “seca” (la lisi de cèl·lules de l'EPR i fotoreceptors i la presència de coriocapilaritis), la US Food and Drug Administration (FDA) ha aprovat aquest any 2023 l'ús intravítri de nous inhibidors del sistema Complement. Es tracta de Pegcetacoplan (SYFOVE; Apellis Pharmaceuticals) un pentadecapèptid pegilat inhibidor de C3/C3b i Avacincaptat pegol (IZERVAY; IVERIC bio) un aptàmer d'ARN pegilat inhibidor de C5.
Pegcetacoplan va ser aprovat al febrer en base als resultats de seguretat i eficàcia obtinguts als assaigs clínics multicèntrics OAKS i DERBY que incloïen el seguiment durant 24 mesos de 1258 pacients ≥60 anys amb una àrea de lesió (foveal i extrafoveal) entre 2,5 i 17,5 mm2. A l'estudi OAKS es va observar una reducció de la taxa mitjana de creixement de la lesió tant en els pacients que van rebre tractament mensual (-21%, P = 0,0003) com bimensual (-16 %, P = 0,0052). A l'estudi DERBY, els pacients amb tractament mensual van mostrar una reducció estadísticament no significativa en el creixement de la lesió encara que superior als que van rebre tractament simulat (-12%, p = 0,0528) o bimensual (-11%, P = 0,075). Els esdeveniments adversos reportats van ser molèstia ocular (13%), DMAE neovascular (12%), mosques volants vítrees (10%) i hemorràgia conjuntival (8%).
Per la seva banda, Avacincaptad pegol va ser aprovat a l'agost sobre la base dels resultats obtinguts per dos assaigs clínics fase 3 (GATHER1 i GATHER2) que incloïen un seguiment de 18 mesos a 624 pacients ≥50 anys amb una àrea de lesió entre 2,5 i 17 ,5 mm2. Avacincaptat pegol mensual va induir una reducció significativa en la taxa mitjana de creixement de la lesió en comparació del grup control (0,292 mm davant 0,402 mm, P = 0,0072), en els primers 12 mesos de tractament cosa que es va mantenir 18 mesos després. Les reaccions adverses reportades en aquests assajos van ser hemorràgia conjuntival (13%), augment de pressió intraocular (9%), visió borrosa (8%) i neovascularització coroïdal (7%).
Analitzant els resultats obtinguts podem dir que l'aprovació de Pegcetacoplan i Avacincaptat pegol per al maneig de la DMAE seca són un bon inici, però encara queda continuar treballant per una millor entesa de la fisiopatologia de la malaltia que permeti oferir noves i més eficients teràpies a aquests pacients les opcions dels quals segueixen encara sent molt limitades. Per acabar, ressenyar que ambdós fàrmacs poden suposar alternatives terapèutiques en altres malalties greus que cursen amb activació del sistema Complement com són l'Hemoglobinúria Paroxística Nocturna (HPN) i la Síndrome hemolítica Urèmica (SHU) el tractament actual de les quals és Eculizumab, un anticòs monoclonal inhibidor C5.
Dra. Jennifer Bolaños Gómez
M.I.R. de segon any en Immunologia
Servei d’Immunologia, Centre de Diagnòstic Biomèdic
Hospital Clínic de Barcelona